Naar een intelligente vorm van diepe hersenstimulatie
Diepe hersenstimulatie (oftewel ‘Deep Brain Stimulation’ – afgekort ‘DBS’) wordt sinds 1997 toegepast bij Parkinsonpatiënten om de symptomen (tremor, spierstijfheid en het moeilijk bewegen) te verminderen. Door een klein gaatje in de schedel plaatst de neurochirurg een dunne draad (de ‘lead’) diep in de hersenen. Via de elektrodecontacten (de huidige leads bestaan uit slechts 4 cylindervormige elektrodecontacten, zie fig. A en B) worden de hersenen lokaal continu elektrisch gestimuleerd. DBS is vaak een laatste mogelijkheid voor het reduceren van symptomen voor Parkinsonpatiënten die niet meer reageren op medicatie of last krijgen van bijwerkingen waardoor de kwaliteit van leven ernstig wordt aangedaan. De ziekte van Parkinson openbaart zich veelal bij oudere mensen en met het vergrijzen van de Nederlandse bevolking zal er daarom steeds meer vraag zijn naar het gebruik van DBS. Het goed lokaliseren van het doelgebied voor stimulatie en het vinden van de juiste instellingen kost veel tijd, zowel tijdens de implantatie als de maanden erna en maakt DBS daarom tot een kostbare therapie die slechts voor een beperkte groep patiënten beschikbaar is.
De stimulator staat vaak dag en nacht aan met dezelfde instellingen, ondanks dat symptomen sterk kunnen fluctueren gedurende de dag. De behandeling wordt dus niet optimaal ingesteld op basis van de toestand van de patiënt. Om DBS intelligenter te maken en selectiever per symptoom toe te passen moet de toestand van de patiënt worden bepaald, bijvoorbeeld door lokaal de hersenaktiviteit te meten en de bewegingen van de patiënt.
Het doel van het onderzoek is op basis van deze metingen de toestand van de patiënt te bepalen evenals de invloed van verschillende stimulatie-instellingen hierop, zodat voor iedere patiënt sneller een optimalere instelling kan worden verkregen. In het onderzoek wordt een nieuw type DBS-lead gebruikt dat wordt ontwikkeld door Sapiens, een in 2011 opgericht nieuw Nederlands bedrijf dat inmiddels deel uit maakt van Medtronic en dat een nieuwe generatie stimulatoren aan het ontwikkelen is voor DBS. Deze lead bestaat uit 40 afzonderlijk aan te sturen elektrodecontacten (zie fig. C). Deze lead maakt het mogelijk het stimulatieveld in een bepaalde richting te kunnen sturen en om de lokale hersenaktiviteit te meten. Model-simulaties laten zien dat er een grotere groep neuronen in de STN kan worden gestimuleerd door gebruik te maken van sturing.
Er zijn testmetingen uitgevoerd bij 8 Parkinsonpatiënten met deze elektrode. De resultaten van deze studie in combinatie met patiënt-specifieke modellen geven ons inzicht in de relatie tussen de aktivatiepatronen en de stimulatie-effecten. Fig. D geeft een voorbeeld van de resultaten van één patient. De combinatie van de data van alle patienten zorgt ervoor dat we in kaart kunnen brengen welke gebieden we voornamelijk moeten stimuleren voor welke symptomen en welke gebieden we moeten vermijden omdat deze zorgen voor bijverschijnselen (fig. E).
De PowerGlove wordt getest voor het kwantificeren van Parkinsonsymptomen (fig. F). Deze ‘handschoen’ kan nauwkeurig handbewegingen meten op basis waarvan bepaalde motorische kenmerken kunnen worden geobserveerd (bijv. tremor en traagheid van bewegen). Aan de hand van metingen aan 35 patiënten die zowel met als zonder medicatie een aantal bewegingstaken hebben uitgevoerd zullen de parameters worden bepaald die een goede afspiegeling geven van de toestand van de patiënt.
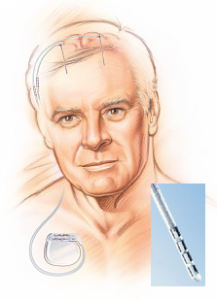
A: Schematische weergave van twee geïmplanteerde DBS-leads. Huidige leads bevatten elk 4 elektrodeconctacten (zie inzet); de pulsgenerator is in de schouderholte geīmplanteerd (Medtronic Inc.).

B: Model-simulatie van de activatie (groen) van neuronen en axonen rondom de Medtronic lead.
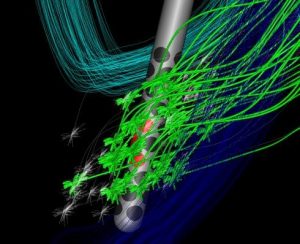
C: De Sapiens lead; de elektrodecontacten die worden aangestuurd voor stimulatie zijn in rood aangegeven. De Sapiens elektrode maakt het mogelijk veel selectiever binnen een hersenstructuur te stimuleren door het stimulatieveld in een bepaalde richting te sturen.


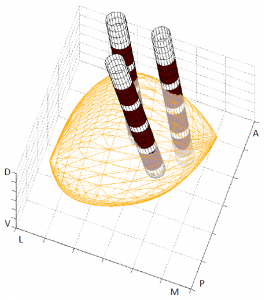
D: Voor twee verschillende stimulatierichtingen (lateraal (links) en mediaal (rechts)) laat het model zien welk gebied in de STN (groen) en welke vezels van de Capsula Interna (IC) (bruin) worden gestimuleerd in een specifieke patient. De stimulatie amplitude is de drempelwaarde waarbij bijwerkingen ontstaan. Stimulatie in laterale richting zorgt in dit geval voor bijwerkingen bij een lagere amplitude (2.5 mA) in vergelijking met mediale stimulatie (3.5 mA); de activatie van de IC speelt hier waarschijnlijk een rol in.
E: Het gebruik van modellen maakt het mogelijk om de positionering van de DBS elektrode in verschillende patiënten met elkaar te vergelijken en de relatie te vinden tussen stimulatiegebied en symptoomreductie.

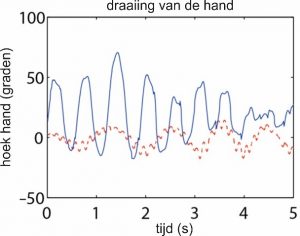
F G
F: De PowerGlove, een ‘handschoen’ waarbij op elk vingersegment een bewegingssensor is gepositioneerd om handbewegingen, zoals draaiingen (G), mee te kunnen meten.
Onderzoeksteam
Universiteit Twente (UT):
Mw. Dr.ir. T. Heida, universitair docent
Ir. K.J. van Dijk, elektrotechnicus en promovendus
Prof.dr.ir. P.H. Veltink, hoogleraar Biomedische Signalen & Systemen en promotor
Academisch Medisch Centrum Amsterdam (AMC):
Dr.ir. L. Bour, klinisch fysicus
R. Verhagen (MSc.), technisch geneeskundige en promovendus
Mw. Dr. M.F. Contarino, neuroloog
Dr. R.M. de Bie, neuroloog
Dr. P.R. Schuurman, neurochirurg
Dr. P. van den Munckhof, neurochirurg
Contactgegevens
Dr.ir. T Heida
Universiteit Twente
Biomedische Signalen & Systemen
TechMed Centre
Postbus 217, 7500 AE Enschede
Tel. 053 4892759
t.heida@utwente.nl
Publicaties
Bot M, Schuurman PR, Odekerken VJJ, Verhagen R, Contarino FM, De Bie RMA, Van den Munckhof P (2018) Deep brain stimulation for Parkinson’s disease: defining the optimal location within the subthalamic nucleus. JNNP 89:493-489
Dijk van KJ, Verhagen R, Bour LJ, Heida C, Veltink PH (2017) Avoiding internal capsule stimulation with a new eight channel steering deep brain stimulation lead, Neuromodulation, doi: 10.1111/ner.12702
Noort van den JC, Verhagen R, Dijk van KJ, Veltink PH, Vos MCPM, Bie de RMA, Bour LJ, Heida T (2017) Quantification of hand motor symptoms in Parkinson’s disease: a proof-of-principle study using inertial and force sensors. Ann Biomed Eng, 1-14
Heida T & Modolo J (2017) Models of Deep Brain Stimulation (2017) Scholarpedia 12, 33311
Bour LJ, Contarino F, Verhagen R, Lourens M, Bie de R, Munckhof van den P, Schuurman R (2016) Is a multi array-contact lead able to improve STN-DBS in Parkinson’s disease? Clin Neurophysiol 127, e2-e3
Verhagen R, Schuurman PR, Van den Munckhof P, Contarino MF, De Bie RMA, Bour L (2016) Comparative study of microelectrode recording-based STN location and MRI-based STN location in low to ultra-high field (7.0 T) T2-weighted MRI images. JNE 13
Bour LJ, Lourens MAJ, Verhagen R, Bie de RMA, Munckhof van den P, Schuurman PR, Contarino MF (2015) Directional recording of subthalamic spetral power densities in Parkinson’s disease and the effect of steering deep brain stimulation. Brain Stim 8, 730-741
Verhagen R, Zwartjes DGM, Heida T, Wiegers EC, Contarino MF, Bie de RMA, Munckhof van den P, Schuurman PR, Veltink PH, Bour LJ (2015) Advanced target identification in STN-DBS with beta power of combined local field potentials and spiking activity. J Neurosci Meth 253, 116-125
Dijk van KJ, Verhagen R, Chaturvedi A, McIntyre CC, Bour LJ, Heida C, Veltink PH (2015) A novel lead design enables selective deep brain stimulation of neural populations in the subthalamic region. J Neural Eng 12. doi:10.1088/1741-2560/12/4/046003
Heida T, Wentink EC, Zhao Y, Marani E (2014) Effects of STN DBS and auditory cueing on the performance of sequential movements and the occurrence of action tremor in Parkinson’s disease. J NeuroEng Rehab doi:10.1186/1743-0003-11-135
Contarino MF, Bour LJ, Verhagen R, Lourens MAJ, Bie de RMA, Munckhof van den P, Schuurman PR (2014) Directional steering: a novel approach to deep brain stimulation, Neurology 83, 1163-1169
Heida T, Wentink EC, Marani E (2013) Power spectral density analysis of physiological, rest and action tremor in Parkinson’s disease patients treated with deep brain stimulation, J Neuroeng Rehab 10:70
Zwartjes DGM, Heida T, Feirabend HKP, Janssen MLF, Visser-Vandewalle V, Martens HCF, Veltink PH (2012) Motor cortex stimulation for Parkinson’s disease: A modeling study. J Neural Eng 9 doi: 10.1088/1741-2560/9/5/056005.
